Nội Dung Chính
Trang 36
MỤC TIÊU
Phân tích được các thành phần của các phần tử phúc chất phổ biến, gồm: nguyên tử trung tâm (callon, nguyên tử trung hoà) và phối tử (anion, phần tử trung hoà), số phối trí của nguyên tử trung tâm; dung lượng phối trí của phối tử.
| MỞ ĐẦU Trong phân tử phức chất, số lượng phối tử cũng như số liên kết cho – nhận giữa phối từ với nguyên tử trung tâm và cấu tạo của phản chất có mối liên hệ như thế nào? |
I. PHỐI TỬ VÀ DUNG LƯỢNG PHỐI TRÍ
1. Nguyên tử tạo liên kết cho – nhận của phối tử
Trong phức chất, các phổi từ cho nguyên tử trung tâm cặp electron hóa trị chưa liên kết để tạo thành liên kết σ theo kiểu cho – nhận. Dựa vào công thức Lewis của phối tử, có thể dự đoán được phối tử liên kết với nguyên tử trung tâm qua nguyên tử nào.
Ví dụ: phân tử H2O có công thức Lewis như sau:
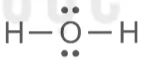
H2O có thể tạo liên kết cho – nhận với nguyên tử trung tâm qua nguyên tử O do nguyên từ O còn hai cặp electron chưa liên kết. Trong công thức cấu tạo của phức chất, người ta biểu diễn liên kết giữa phối tử với nguyên tử trung tâm bằng gạch nối từ nguyên tử cho cặp electron của phối tử đến nguyên tử trung tâm.
Ví dụ: Liên kết giữa H2O và Cu2+ trong phức chất [Cu(H2O)62+ được biểu diễn như sau:
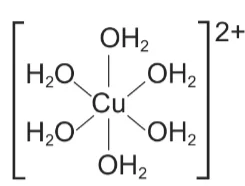
Hoạt động nghiên cứu
Viết công thức Lowis của NH3 và OH-. Cho biết NH3 và OH- có thể liên kết với nguyên tử trung tâm trong phức chất qua nguyên tử nào.
Trang 37
2. Dung lượng phối trí của phối tử
Phối tử có thể liên kết với nguyên tử trung tâm qua một hoặc nhiều nguyên tử bằng một hoặc nhiều liên kết cho - nhận tương ứng. Số liên kết ở của một phối tử với nguyên tử trung tâm được gọi là dung lượng phối trí của phối tử đó.
Phối tử liên kết với nguyên tử trung tâm chỉ qua một nguyên tử có dung lượng phối trí là 1.
Ví dụ: H2O trong phức chất [Cu(H2O)6]2+ có dung lượng phối trí là 1 vì chỉ liên kết với nguyên tử trung tâm Cu2+ qua một nguyên tử O.
Phối tử liên kết với nguyên tử trung tâm qua 2, 3, 4.... nguyên tử có dung lượng phối trí là 2, 3, 4,... tương ứng. Các phối tử này thường tạo ra phức chất vòng bên.
Ví dụ: Phức chất [PICI2(en)] có vòng 5 cạnh bền:
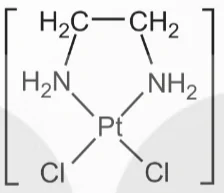
Phối tử ethylenediamine (en) có dung lượng phối trí là 2 vì liên kết với nguyên tử trung tâm Pt2+ qua hai nguyên tử N.
EM CÓ BIẾT
Phối tử có dung lượng phối trí là 1 còn được gọi là phối tù đơn càng. Phối tử có dung lượng phối trí từ 2 trở lên được gọi là phối tử đa càng. Phối tử có dung lượng phối trí là 2, 3, 4,... được gọi tương ứng là phối tử hai càng, phối từ ba càng, phối tử bốn càng,...
Bảng 7.1. Một số phối tử và dung lượng phối trí phổ biến
| Phối tử | Dung lượng phối trí | Ví dụ |
| H2O | 1 | [Cu(H2O)6]2+ |
| NH3 | 1 | [Ni(NH3)6]2+ |
| Cl- | 1 | [ZnCl4]2- |
| OH- | 1 | [Al(OH)4]- |
| H2NCH2CH2NH2 | 2 | [Cu(en)2]2+ |
Hoạt động nghiên cứu
Hãy cho biết dung lượng phối trí của mỗi phối tử trong phim chất [PtCl2(en)]2+.
Trang 38
II. NGUYÊN TỬ TRUNG TÂM VÀ SỐ PHỐI TRÍ CỦA NGUYÊN TỬ TRUNG TÂM
Trong phức chất, tổng số liên kết ở giữa nguyên tử trung tâm với các phối tử được gọi là số phối trí của nguyên tử trung tâm đó.
Số phối trí của nguyên tử trung tâm thường là 2, 4 và 6, tuỳ thuộc vào bản chất của nguyên tử trung tâm và phối tử.
Bảng 7.2. Số phối trí của nguyên tử trung tâm trong một số phức chất
| Phức chất | Nguyên tử trung tâm | Số phối trí của nguyên tử trung tâm | Phức chất | Nguyên tử trung tâm | Số phối trí của nguyên tử trung tâm |
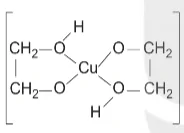 | Cu2+ | 4 | 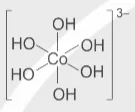 | Co3+ | 6 |
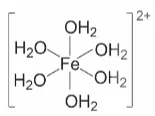 | Fe2+ | 6 | 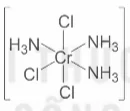 | Cr3+ | 6 |
Hoạt động nghiên cứu
Cho các phúc chất A, B, C, D sau:
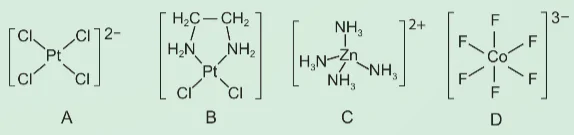
Xác định số phối trí của nguyên tử trung tâm trong mỗi phức chất trên.
Trang 39
EM ĐÃ HỌC
• Dung lượng phối trí của một phối tử là số liên kết ở giữa phối tử đó với nguyên tử trung tâm.
• Số phối trí của nguyên tử trung tâm là tổng số liên kết ở giữa nguyên từ trung tâm với các phối tử trong phức chất.
EM CÓ THỂ
Xác định được số phối trí của nguyên tử trung tâm và dung lượng phối trí của phối tử trong một phức chất khi biết công thức cấu tạo của phức chất đó.


































































Bình Luận
Để Lại Bình Luận Của Bạn