Nội Dung Chính
(Trang 51)
Học xong bài học này, em có thể:
• Nêu được khái niệm base (tạo ra ion OH
• Nêu được kiềm là các hydroxide tan tốt trong nước.
• Tiến hành được thí nghiệm base là làm đổi màu chất chỉ thị, phản ứng với acid tạo muối, nêu và giải thích được hiện tượng xảy ra trong thí nghiệm (viết phương trình hoá học) và rút ra nhận xét về tính chất của base.
• Tra được bảng tính tan để biết một hydroxide cụ thể thuộc loại kiềm hoặc base không tan.
![]() Để tránh nguyên liệu bị nát vụn khi chế biến, trong quá trình làm mứt người ta thường ngâm nguyên liệu vào nước vôi trong. Trong quá trình đó, độ chua của một số loại quả sẽ giảm đi. Vì sao lại như vậy?
Để tránh nguyên liệu bị nát vụn khi chế biến, trong quá trình làm mứt người ta thường ngâm nguyên liệu vào nước vôi trong. Trong quá trình đó, độ chua của một số loại quả sẽ giảm đi. Vì sao lại như vậy?

Hình 9.1. Cà chua được ngâm trong nước vôi để làm mứt
I. KHÁI NIỆM BASE
Base là những hợp chất trong phân tử có nguyên tử kim loại liên kết với nhóm hydroxide. Khi tan trong nước, base tạo ra ion OH .
.
| Ví dụ: NaOH → Na Sodium hydroxide Ion sodium Ion hydroxide Calcium hydroxide Ion calcium Ion hydroxide Tên gọi và công thức hoá học của một số base thông dụng được trình bày trong bảng 9.1. | 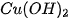 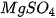 , ,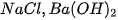 ? ? |
Bảng 9.1. Tên gọi và công thức hoá học của một số base thông dụng
| Tên gọi | Công thức hoá học |
| Potassium hydroxide | KOH |
| Magnesium hydroxide | 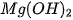 |
| Copper(II) hydroxide | 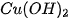 |
(Trang 52)
II. PHÂN LOẠI BASE
Base được chia thành hai loại chính: base tan và base không tan trong nước.
Base tan trong nước còn được gọi là kiềm. Ví dụ: NaOH, KOH,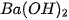
Tính tan của các base trong nước được trình bày trong bảng tính tan (xem Phụ lục).
|
|
Hình 9.2. Dung dịch NaOH |
Hình 9.3. Một số base không tan trong nước |
III. TÍNH CHẤT HOÁ HỌC
1. Làm đổi màu chất chỉ thị
Tiến hành thí nghiệm sau để tìm hiểu về sự làm đổi màu chất chỉ thị của dung dịch base.![]() Thí nghiệm 1
Thí nghiệm 1
Chuẩn bị
• Dụng cụ: Giá để ống nghiệm, ống nghiệm, ống hút nhỏ giọt, mặt kính đồng hồ.
• Hoá chất: Dung dịch NaOH loãng, giấy quỳ tím, dung dịch phenolphthalein.
Tiến hành
• Đặt giấy quỳ tím lên mặt kính đồng hồ, lấy khoảng 1 mL dung dịch NaOH cho vào ống nghiệm.
• Nhỏ một giọt dung dịch NaOH lên mẩu giấy quỳ tím, nhỏ một giọt dung dịch phenolphthalein vào ống nghiệm có dung dịch NaOH.
• Mô tả các hiện tượng xảy ra.
|
a) quỳ tím. b) phenolphthalein. | Các dung dịch base khác cũng làm đổi màu quỳ tím và phenolphthalein tương tự NaOH. Dung dịch base làm quỳ tím chuyển sang màu xanh, phenolphthalein không màu chuyển sang màu hồng. Quỳ tím và phenolphthalein được dùng làm chất chỉ thị màu để nhận biết dung dịch base. |
(Trang 53)
2. Tác dụng với acid
Tiến hành các thí nghiệm sau để tìm hiểu phản ứng của dung dịch base với dung dịch acid.
![]() Thí nghiệm 2
Thí nghiệm 2
Chuẩn bị
• Dụng cụ: Giá để ống nghiệm, ống nghiệm, ống hút nhỏ giọt.
• Hoá chất: Dung dịch NaOH loãng, dung dịch HCl loãng, dung dịch phenolphthalein.
Tiến hành
• Cho khoảng 1 mL dung dịch NaOH vào ống nghiệm, thêm tiếp một giọt dung dịch phenolphthalein và lắc nhẹ.
• Nhỏ từ từ dung dịch HCl loãng vào ống nghiệm đến khi dung dịch trong ống nghiệm mất màu thì dừng lại.
• Mô tả các hiện tượng xảy ra.
• Giải thích sự thay đổi màu của dung dịch trong ống nghiệm trong quá trình thí nghiệm.
Sodium hydroxide tác dụng với hydrochloric acid tạo ra sodium chloride và nước theo
phương trình hoá học:
NaOH + HCl → NaCl + 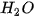
Sodium hydroxide Sodium chloride
![]() Thí nghiệm 3
Thí nghiệm 3
Chuẩn bị
• Dụng cụ: Giá để ống nghiệm, ống nghiệm, ống hút nhỏ giọt, thìa thuỷ tinh.
• Hoá chất: 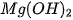 (được điều chế sẵn), dung dịch HCl, nước cất.
(được điều chế sẵn), dung dịch HCl, nước cất.
Tiến hành
• Lấy một lượng nhỏ 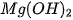 cho vào ống nghiệm, thêm vào khoảng 1 mL nước cất, lắc nhẹ.
cho vào ống nghiệm, thêm vào khoảng 1 mL nước cất, lắc nhẹ.
• Tiếp tục nhỏ từ từ dung dịch HCl vào ống nghiệm đến khi không nhìn thấy chất rắn trong ống nghiệm thì dừng lại.
• Mô tả các hiện tượng xảy ra.
• Giải thích các hiện tượng diễn ra trong quá trình thí nghiệm.
(Trang 54)
|
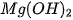 lần lượt tác dụng với: lần lượt tác dụng với: a) dung dịch acid HCI. b) dung dịch acid
| Magnesium hydroxide tác dụng với hydrochloric acid tạo ra magnesium chloride và nước theo phương trình hoá học: Magnesium hydroxide Magnesium chloride Các base khác như: KOH, Base tác dụng với dung dịch acid tạo ra muối và nước.
a) b) c) Em có biết Sodium hydroxide (NaOH) là một trong những hoá chất được sử dụng phổ biến nhất trong phòng thí nghiệm và trong công nghiệp. Phần lớn lượng sodium hydroxide sản xuất ra được sử dụng trong công nghiệp để sản xuất giấy, nhôm, chất tẩy rửa, các muối sodium,... |
 • Base là những hợp chất trong phân tử có nguyên tử kim loại liên kết với nhóm hydroxide. Khi tan trong nước, base tạo ra ion OH
• Base là những hợp chất trong phân tử có nguyên tử kim loại liên kết với nhóm hydroxide. Khi tan trong nước, base tạo ra ion OH
• Base tan trong nước được gọi là kiềm.
• Dung dịch base làm quỳ tím chuyển sang màu xanh, phenolphthalein không màu chuyển sang màu hồng.
• Base tác dụng với dung dịch acid tạo thành muối và nước.
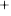 + OH
+ OH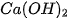 →
→ 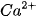 + 2OH
+ 2OH 1. Dựa vào bảng tính tan, cho biết những base nào dưới đây là kiềm: KOH,
1. Dựa vào bảng tính tan, cho biết những base nào dưới đây là kiềm: KOH, 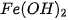 ,
, 

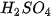 .
.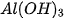 và
và 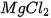 +
+ 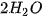
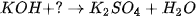
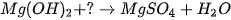




















Bình Luận
Để Lại Bình Luận Của Bạn