Nội Dung Chính
(Trang 32)
Học xong bài học này, em có thể:
• Tính được lượng chất trong phương trình hoá học theo số mol, khối lượng hoặc thể tích ở điều kiện 1 bar và 25 °C.
• Nêu được khái niệm hiệu suất của phản ứng và tính được hiệu suất của một phản ứng dựa vào lượng sản phẩm thu được theo lí thuyết và lượng sản phẩm thu được theo thực tế.

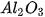 ). Làm thế nào tính được khối lượng nguyên liệu cần dùng để sản xuất nhôm hoặc tính khối lượng nhôm tạo ra nếu biết khối lượng nguyên liệu đã dùng?
). Làm thế nào tính được khối lượng nguyên liệu cần dùng để sản xuất nhôm hoặc tính khối lượng nhôm tạo ra nếu biết khối lượng nguyên liệu đã dùng?I. XÁC ĐỊNH KHỐI LƯỢNG, SỐ MOL CỦA CHẤT PHẢN ỨNG VÀ SẢN PHẨM TRONG PHẢN ỨNG HOÁ HỌC
Ví dụ
Trong phòng thí nghiệm, người ta có thể điều chế khí hydrogen (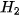 ) bằng cách cho zine tác dụng với dung dịch acid HCl theo phương trình hoá học sau:
) bằng cách cho zine tác dụng với dung dịch acid HCl theo phương trình hoá học sau:
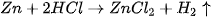
Tính khối lượng acid HCl tham gia phản ứng và thể tích khí 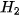 (đkc) thu được khí hoà tan 1,3 gam zinc.
(đkc) thu được khí hoà tan 1,3 gam zinc.
| Số mol của Zn tham gia phản ứng:
Từ phương trình hoá học ta có: Zn + 2HCl → 1 nguyên tử Zn + 2 phân tử HCl → 1 phân tử N nguyên tử Zn + 2N phân tử HCI → N phân tử 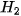 Tức là: 1 mol Zn tác dụng với 2 mol HCl tạo ra 1 mol |
(Trang 33)
| Vậy tỉ lệ số nguyên tử, phân tử của các chất trong phương trình hoá học chính là
Vậy: 0,02 mol Zn tác dụng với 0,02 × 2 = 0,04 mol HCl và tạo ra 0,02 mol • Khối lượng acid HCl phản ứng là:
• Thể tích khí
|
| Để tính khối lượng và số mol của chất phản ứng và chất sản phẩm trong một phản ứng hoá học, ta thực hiện theo các bước sau : Bước 1: Viết phương trình hoá học của phản ứng. Bước 2: Tính số mol chất đã biết dựa vào khối lượng hoặc thể tích. Bước 3: Dựa vào phương trình hoá học và số mol chất đã biết để tìm số mol chất tham gia phản ứng hoặc chất sản phẩm. Bước 4: Tính khối lượng hoặc thể tích của chất cần tìm.
|
Lập phương trình hoá học của phản ứng rồi tính: a) Khối lượng aluminium oxide tạo ra. b) Thể tích khí oxygen tham gia phản ứng ở điều kiện chuẩn. |
II. HIỆU SUẤT PHẢN ỨNG
1. Chất phản ứng hết, chất phản ứng dư
| Đốt cháy hydrogen tạo ra nước theo phản ứng: Số phân tử: 2 phân tử 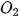 → 2 phân tử → 2 phân tử 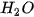 Số mol: 2 mol Như vậy, 2 phân tử |
(Trang 34)
| Em có biết Trong các động cơ ô tô, xe máy chạy bằng xăng, dầu xảy ra phản ứng đốt cháy nhiên liệu. Nhiệt toả ra của phản ứng cháy này được chuyển thành năng lượng giúp xe di chuyển. Người ta cần chế tạo sao cho nhiên liệu và oxygen phản ứng với nhau vừa đủ vì nếu dư oxygen hoặc nhiên liệu đều tạo ra các chất gây ô nhiễm môi trường. Để giải quyết vấn đề đó, các kĩ sư chế tạo máy đã sử dụng cảm biến oxygen để xác định lượng oxygen còn lại trong khí thải, từ đó điều chỉnh lượng nhiên liệu hợp lí.
Thiết bị cảm biến oxygen
|
Hình 5.1. Sơ đồ mô tả số lượng phân tử chất trước và sau phản ứng
Như vậy, sau phản ứng 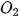 . .
• Chất phản ứng hết là chất không còn sau khi phản ứng kết thúc. • Chất phản ứng dư là chất còn lại sau khi kết thúc phản ứng. 2. Hiệu suất phản ứngĐốt cháy than (thành phần chính là carbon) trong oxygen hoặc trong không khí sinh ra khí carbon dioxide:
Theo phương trình hoá học: nếu đốt 1 mol carbon (tương ứng với 12 gam carbon) trong 1 mol oxygen thì thu được 1 mol 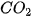 ). Đó là khối lượng tính theo lí thuyết của ). Đó là khối lượng tính theo lí thuyết của 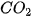 . . Tuy nhiên, thực tế khối lượng Hiệu suất phản ứng (kí hiệu là H) là tỉ số giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo là thuyết.
b) Khi nào hiệu suất của phản ứng bằng 100%? | ||||||||||||
(Trang 35)
| Thông thường, hiệu suất phản ứng biểu thị theo phần trăm và được tính theo biểu thức :
Trong đó:
H là hiệu suất phản ứng (%). Ví dụ : Nếu đốt 12 gam carbon trong oxygen dư thu được 39,6 gam Hiệu suất phản ứng thường nhỏ hơn 100%. Nếu hiệu suất phản ứng là 100% tức là phản ứng hoá học xảy ra hoàn toàn.
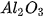 ) theo phương trình hoá học sau: ) theo phương trình hoá học sau:
a) Tính hiệu suất phản ứng khi điện phân 102 kg b*) Biết khối lượng aluminium thu được sau điện phân là 54 kg và hiệu suất phản ứng là 92%, tính khối lượng | Em có biết Khi đốt cháy than trong không khí, sản phẩm thu được chủ yếu là khí carbon dioxide. Nếu lượng oxygen trong không khí thiếu thì sẽ xảy ra phản ứng phụ, tạo ra carbon monoxide (CO) là khí độc. Do đó, các viên than tổ ong được sản xuất với nhiều lỗ để thông khí giúp cung cấp đủ oxygen và tăng diện tích tiếp xúc, góp phần tăng hiệu suất phản ứng đốt cháy than. |
![]()
Bước 1: Viết phương trình hoá học của phản ứng.
Bước 2: Tính số mol chất đã biết dựa vào khối lượng hoặc thể tích.
Bước 3: Dựa vào phương trình hoá học để tìm số mol chất tham gia hoặc chất sản phẩm.
Bước 4: Tính khối lượng hoặc thể tích của chất cần tìm.
• Hiệu suất phản ứng là tỉ số giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lí thuyết.
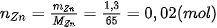
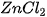 +
+ 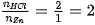 ;
; 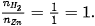
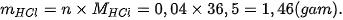
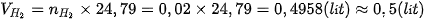

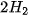 +
+ 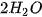

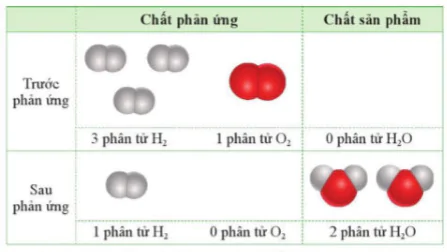
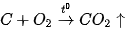
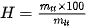
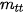 là khối lượng chất (g) thu được theo thực tế.
là khối lượng chất (g) thu được theo thực tế.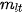 là khối lượng chất (g) thu được theo lí thuyết ( tính theo phương trình).
là khối lượng chất (g) thu được theo lí thuyết ( tính theo phương trình).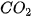 thì hiệu suất phản ứng là :
thì hiệu suất phản ứng là :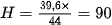 (%)
(%) 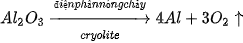
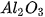 , biết khối lượng nhôm thu được sau phản ứng là 51,3 kg.
, biết khối lượng nhôm thu được sau phản ứng là 51,3 kg.
























Bình Luận
Để Lại Bình Luận Của Bạn