Nội Dung Chính
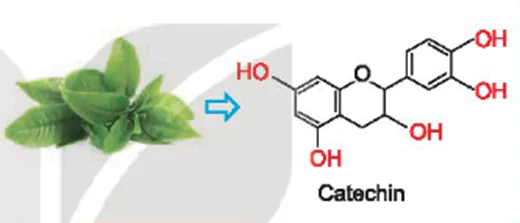
Mở đầu trang 129 Hóa học 11: Catechin là một hợp chất phenol có trong lá chè xanh. Catechin có tác dụng chống oxi hoá, diệt khuẩn, kháng viêm, ngăn ngừa một số bệnh về tim mạch, cao huyết áp, tiêu hoá, làm chậm quá trình lão hoá, … Vậy hợp chất phenol là gì và có các tính chất đặc trưng nào?
Lời giải:
- Phenol là những hợp chất hữu cơ trong phân tử có nhóm – OH liên kết trực tiếp với nguyên tử carbon của vòng benzene.
- Phenol có các tính chất hoá học đặc trưng:
+ Tham gia phản ứng thế nguyên tử H của nhóm – OH (tính acid).
+ Tham gia phản ứng thế ở vòng thơm.
IV. Tính chất hoá học
Hoạt động trang 131 Hóa học 11: Nghiên cứu phản ứng của phenol với dung dịch NaOH và dung dịch Na2CO3
Thí nghiệm phenol tác dụng với dung dịch NaOH và với dung dịch Na2CO3 được tiến hành như sau:
- Cho vào hai ống nghiệm, mỗi ống nghiệm khoảng 1 mL dung dịch phenol bão hoà (có màu trắng đục).
- Cho khoảng 1 mL dung dịch NaOH 2 M vào ống nghiệm (1) và lắc đều.
- Cho khoảng 1 mL dung dịch Na2CO3 2 M vào ống nghiệm (2) và lắc đều.
Cả hai ống nghiệm đều quan sát được dung dịch từ màu trắng đục chuyển sang trong suốt.
Hãy giải thích các hiện tượng xảy ra.

Lời giải:
Hiện tượng: Ở cả hai ống nghiệm dung dịch từ màu trắng đục chuyển sang trong suốt.
Giải thích:
- Phenol ít tan trong nước ở điều kiện thường do đó ban đầu dung dịch có màu trắng đục;
- Phenol phản ứng với các dung dịch NaOH, Na2CO3 tạo thành các muối tan nên sau phản ứng thu được dung dịch trong suốt.
Phương trình hoá học:
C6H5OH + NaOH → C6H5ONa + H2O
C6H5OH + Na2CO3 ⇌ C6H5ONa + NaHCO3.
Câu hỏi 1 trang 131 Hóa học 11: Hãy giải thích tại sao phenol có thể phản ứng được với dung dịch NaOH còn alcohol thì không phản ứng với dung dịch NaOH.
Lời giải:
Trong dung dịch nước, phenol phân li theo cân bằng sau:
C6H5OH + H2O ⇌ C6H5O− + H3O+
Do đó, phenol là một acid yếu, có thể tác dụng được với dung dịch NaOH.
Alcohol là chất không điện li, nên không có khả năng phân li như phenol nên không tác dụng với NaOH.
Hoạt động trang 131 Hóa học 11: Phản ứng của phenol với nước bromine
Phản ứng của phenol với nước bromine được tiến hành như sau:
- Cho khoảng 1,0 mL dung dịch phenol 5% vào ống nghiệm.
- Nhỏ vài giọt nước bromine bão hoà vào ống nghiệm, lắc đều. Nước bromine mất màu và xuất hiện kết tủa trắng.
Hãy giải thích hiện tượng xảy ra và viết phương trình hoá học của phản ứng.
Lời giải:
Hiện tượng: Nước bromine mất màu và xuất hiện kết tủa trắng do phenol phản ứng với nước bromine tạo thành sản phẩm thế 2,4,6 – tribromophenol ở dạng kết tủa màu trắng.
Phương trình hoá học:
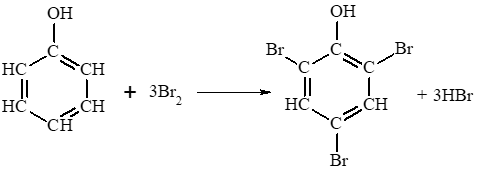
Câu hỏi 2 trang 132 Hóa học 11: So sánh điều kiện phản ứng bromine hoá vào vòng benzene của phenol và benzene. Từ đó, rút ra nhận xét khả năng thế nguyên tử hydrogen của vòng benzene của phenol so với benzene.
Lời giải:
Benzene phản ứng với Br2 trong điều kiện đun nóng và có xúc tác FeBr3. Phenol phản ứng với Br2 ngay điều kiện thường và không cần chất xúc tác. Điều đó chứng tỏ do ảnh hưởng của nhóm – OH, phản ứng thế nguyên tử hydrogen ở vòng benzene của phenol xảy ra dễ dàng hơn so với benzene.
Câu hỏi 3 trang 132 Hóa học 11: Viết phương trình hoá học của phản ứng xảy ra khi cho 4 – methylphenol tác dụng với nước bromine.
Lời giải:
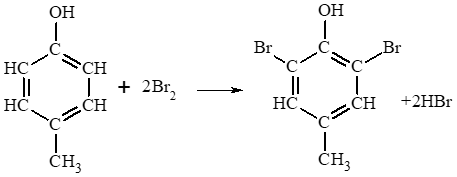
Hoạt động trang 132 Hóa học 11: Nghiên cứu phản ứng nitro hoá phenol – tổng hợp picric acid
Thí nghiệm nitro hoá phenol được tiến hành như sau:
- Cho 0,5 g phenol và khoảng 1,5 mL H2SO4 đặc vào ống nghiệm, đun nhẹ hỗn hợp trong khoảng 10 phút để thu được chất lỏng đồng nhất.
- Để nguội ống nghiệm rồi ngâm bình trong cốc nước đá.
- Nhỏ từ từ 3 mL dung dịch HNO3 đặc vào hỗn hợp và lắc đều. Nút bằng bông tẩm dung dịch NaOH.
- Đun cách thuỷ hỗn hợp trong nồi nước nóng 15 phút.
- Làm lạnh hỗn hợp rồi đem pha loãng hỗn hợp với khoảng 10 mL nước cất, picric acid kết tủa ở dạng tinh thể màu vàng.
Hãy giải thích hiện tượng xảy ra và viết phương trình hoá học của phản ứng.
Chú ý: Thí nghiệm thực hiện trong tủ hốt hoặc nơi thoáng khí. Cần thận trọng khi làm việc với dung dịch HNO3 đặc và dung dịch H2SO4 đặc.
Lời giải:
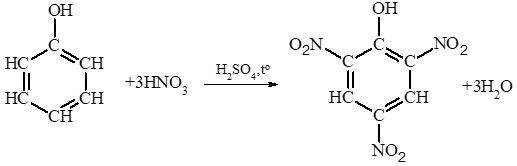
Phenol phản ứng với dung dịch nitric acid đặc trong dung dịch sulfuric acid đặc tạo ra sản phẩm 2,4,6 – trinitrophenol (picric acid, dạng tinh thể màu vàng).
Phương trình hoá học:
VI. Điều chế
Hoạt động trang 133 Hóa học 11: Sưu tầm, tìm hiểu thông tin và trình bày một số ứng dụng của phenol trong đời sống và sản xuất.
Lời giải:
Phenol được sử dụng nhiều trong công nghiệp hoá chất và y học.
Phenol là nguyên liệu chính để sản xuất bisphenol A, một chất trung gian dùng trong sản xuất nhựa epoxy. Phenol cũng được sử dụng nhiều trong sản xuất nhựa phenol – formaldehyde hay poly(phenol – formaldehyde).
Phenol được dùng để sản xuất phẩm nhuộm, sản xuất thuốc nổ (2,4,6 – trinitrophenol), chất diệt cỏ 2,4 – D (2,4 – dichlorophenoxyacetic acid); chất diệt nấm mốc (các đồng phân của nitrophenol),…
Do có tính diệt khuẩn nên phenol được dùng làm chất khử trùng, tẩy uế. Thuốc xịt chloraseptic chứa 1,4% phenol được dùng làm thuốc chữa đau họng.
Em có thể trang 133 Hóa học 11: Sưu tầm một số sản phẩm có phenol trong thành phần để trình bày về các ứng dụng đa dạng của phenol trong cuộc sống.
Lời giải:
Một số sản phẩm có phenol trong thành phần:








































































Bình Luận
Để Lại Bình Luận Của Bạn