Nội Dung Chính
(Trang 136)
MỤC TIÊU
- Nêu được khái niệm hợp chất carbonyl (aldehyde và ketone).
- Gọi được tên theo danh pháp thay thế một số hợp chất carbonyl đơn giản (C1-C5), tên thông thường một vài hợp chất carbonyl thường gặp.
- Mô tả được đặc điểm liên kết của nhóm chức carbonyl, hình dạng phân tử của methanal, ethanal.
- Nêu được đặc điểm về tính chất vật lí (trạng thái, nhiệt độ sôi, tính tan) của hợp chất carbonyl.
- Trình bày được tính chất hoá học của aldehyde, ketone: phản ứng khử (với NaBH4, hoặc LiAIH4; phản ứng oxi hoá aldehyde (với nước bromine, thuốc khử Tollens, Cu(OH)2/OH-); phản ứng cộng vào nhóm carbonyl (với HCN); phản ứng tạo iodoform.
- Thực hiện được (hoặc quan sát qua video, hoặc qua mô tả) các thí nghiệm: phản ứng tráng bạc, phản ứng với Cu(OH)2/OH, phản ứng tạo iodoform từ acetone; mô tả hiện tượng thí nghiệm, giải thích tính chất hoá học của hợp chất carbonyl và xác định hợp chất có chứa nhóm CH3CO-.
- Trình bày được ứng dụng của hợp chất carbonyl và phương pháp điều chế acetaldehyde bằng cách oxi hoá ethylene, điều chế acetone từ cumene.
| Mở đầu Các aldehyde, ketone tạo nên mùi thơm đặc trưng của các loài động vật và thực vật. Nhiều aldehyde, ketone đóng vai trò quan trọng đối với cơ thể: tế bào trong võng mạc giúp mắt tiếp nhận ánh sáng được tạo thành thành từ từ aldehyde, aldehyde, các các hormone hormone gio giới tính nam và nữ là các ketone. Vậy, họp chất carbonyl là gì và chúng có những tinh chất nào? |
I. KHÁI NIỆM, DANH PHÁP
1. Khái niệm
Hợp chất carbonyl là các hợp chất hữu cơ trong phân tử có chứa nhóm chức carbonyl 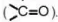
Aldehyde là hợp chất hữu cơ có nhóm -CHO liên kết với nguyên tử carbon (trong gốc hydrocarbon hoặc –CHO) hoặc nguyên tử hydrogen.
Ketone là hợp chất hữu cơ có nhóm 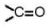 liên kết với hai gốc hydrocarbon.
liên kết với hai gốc hydrocarbon.
(Trang 137)
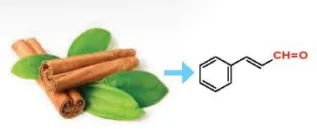
Hình 23.1. Cinnamaldehyde là một hợp chất aldehyde có trong tinh dầu quế

Hình 23.2. Menthone là một hợp chất ketone có trong tinh dầu bạc hà
| EM CÓ BIẾT Trong tự nhiên, các hợp chất chứa nhóm chức aldehyde và ketone tồn tại khá phổ biến trong tinh dầu của nhiều loài cây cỏ. Ví dụ:
citronellal (tinh dầu chanh)
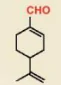
perillaldehyde (tinh dầu tía tô)
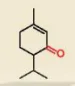
piperitone (tinh dầu khuynh diệp) CHO CHO CHO |
2. Danh pháp
a) Danh pháp thay thế
Tên gọi theo danh pháp thay thế của aldehyde đơn chức và ketone đơn chức:
Tên aldehyde
Ví dụ: CH3-CH2-CH=O
Tên ketone
Ví dụ: 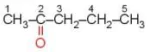
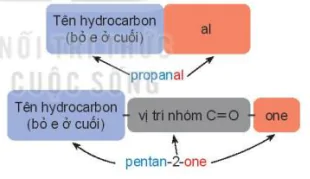
Tên hydrocarbon (bỏ e ở cuối)
al
propanal
Tên hydrocarbon (bỏ e ở cuối)
vị trí nhóm C=O
one
pentan-2-one
Chú ý:
- Mạch carbon là mạch dài nhất chứa nhóm 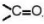 .
.
- Mạch carbon được đánh số từ nhóm -CHO (đối với aldehyde) hoặc từ phía gần nhóm 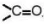
- Đối với ketone, nếu nhóm 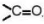 chỉ có một vị trí duy nhất thì không cần số chỉ vị trínhóm
chỉ có một vị trí duy nhất thì không cần số chỉ vị trínhóm 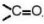 .
.
- Nếu mạch carbon có nhánh thì cần thêm vị trí và tên nhánh ở phía trước.
(Trang 138)
Ví dụ: 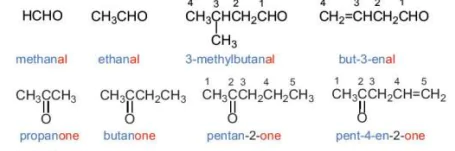
HCHO
methanal
propanone
CH3CHO
ethanal
butanone
3-methylbutanal
pentan-2-one
but-3-enal
pent-4-en-2-one
b) Tên gọi thông thường
Một số aldehyde, ketone đơn giản được gọi theo tên thông thường có nguồn gốc lịch sử. Tên thông thường của các aldehyde có nguồn gốc từ tên của acid tương ứng.
Ví dụ:
HCHO
andehit formic
(formaldehyde)
CH3CHO
aldehyt axetic
(acetaldehyde)
C6H5CHO
aldehyd benzoic
(benzaldehyde)
CH3COCH3
acetone
| CÂU HỎI VÀ BÀI TẬP 1. Viết các công thức cấu tạo và gọi tên theo danh pháp thay thế của hợp chất carbonyl có công thức phân tử C4H8O 2. Viết công thức cấu tạo của các hợp chất carbonyl có tên gọi dưới đây: a) propanal; b) 3-metylbut-2-enal; c) pentan-2-one; d) 3-metylbutan-2-on. |
II. ĐẶC ĐIỂM CẤU TẠO
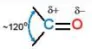
Liên kết đôi C=O phân cực về phía nguyên tử oxygen (Hình 23.3).
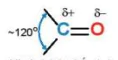
Hình 23.3. Cấu trúc nhóm carbonyl
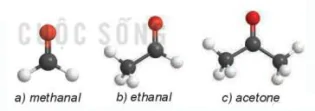
Hình 23.4. Mô hình phân tử của một số hợp chất carbonyl
a) methanal
b) etanol
c) axeton
III. TÍNH CHẤT VẬT LÍ
| Hoạt động nghiên cứu Cho biết các hợp chất dưới đây có khối lượng phân tử gần tương đương nhau và có nhiệt độ sôi như sau:
CH3CH2CH2CH3 CH3CH2CHO CH3CH2CH2OH ts (° C): -0,5 49 97,1 So sánh nhiệt độ sôi của hợp chất carbonyl với alkane và alcohol có khối lượng phân tử tương đương. Dựa vào khả năng tạo liên kết hydrogen và sự phân cực của phân tử đề giải thích. |
(Trang 139)
Các aldehyde, ketone có nhiệt độ sôi cao hơn các hydrocarbon có khối lượng phân tử tương đương do trong phân tử chứa nhóm carbonyl phân cực làm cho phân tửaldehyde, ketone phân cực nên có nhiệt độ sôi cao hơn.
Ở nhiệt độ thường, các aldehyde có phân tử khối nhỏ (methanal, ethanal) ở trạng thái khí, các hợp chất carbonyl thông dụng khác ở trạng thái lỏng.
Các aldehyde, ketone có mạch carbon ngắn tan tốt trong nước. Khi số nguyên tửcarbon tăng thì độ tan của hợp chất carbonyl giảm dần.
Bảng 23.1. Nhiệt độ sôi và tính tan của một số hợp chất carbonyl (1)
| Công thức | Tên | Nhiệt độ sôi (°C) | Độ tan trong nước ở 20 °C (g/100 g) | |
| aldehyde | HCHO | methanal | -21 | tan vô hạn |
| CH3CHO | Ethanal | 20 | tan vô hạn | |
| CH3CH2CHO | propanal | 49 | 20 | |
| CH3CH2CH2CHO | butanal | 76 | 7 | |
| ketone | CH3COCH3 | propanone | 56 | tan vô hạn |
| CH3COCH2CH3 | butanone | 80 | 26 | |
| CH3CH2COCH2CH3 | pentan-3-one | 101 | 5 | |
IV. TÍNH CHẤT HOÁ HỌC
1. Phản ứng khử
Các hợp chất carbonyl bị khử bởi các tác nhân khử như NaBH4, LiAlH4.... (kí hiệu: [H]) tạo gung: J ứng: aldehyde bị khử tạo thành alcohol t thành các alcohol tương ứng: aldehyde bị khử tạo thành alcohol bậc I, ketone bị khửtạo thành alcohol bậc II.
Ví dụ: 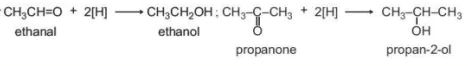
ethanal
ethanol
propanone
propan-2-ol
| CÂU HỎI VÀ BÀI TẬP 3. Khử các hợp chất carbonyl sau bởi NaBH4, hãy viết công thức cấu tạo của các sản phẩm: a) propanal; b) 2-methylbutanal; c) butanone; d) 3-methylbutan-2-one. |
(1) Nguồn: Organic chemistry, William H. Brown, Cengage Learning, 2018.
(Trang 140)
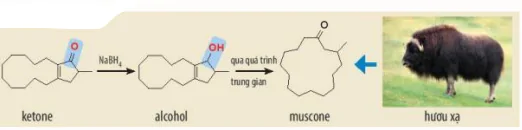
| EM CÓ BIẾT Muscone là hợp chất ketone tạo nên mùi thơm đặc trưng của xạ hương và được sử dụng phổ biến trong công nghiệp nước hoa, mỹ phẩm và y học. Trước đây, xạ hương tự nhiên được lấy từ tuyến thơm của hươu xạ. Tuy nhiên, để bảo vệ loài hươu xạ, ngày nay xạ hương được tổng hợp bằng con đường hoá học. Dưới đây là một phương pháp tổng hợp muscone, trong đó giai đoạn đầu là phản ứng khử hợp chất ketone thành alcohol bởi tác nhân khử NaBH.
NaBH4 OH through the process intermediate ketone alcohol muscone hươu xạ |
2. Phản ứng oxi hoá aldehyde
Aldehyde dễ bị oxi hoá bởi các tác nhân oxi hoá thông thường như: Br2/H2O, [Ag(NH3)2]OH, Cu(OH)2/OH-....
a) Oxi hoá aldehyde bởi nước bromine
Aldehyde bị oxi hoá bởi nước bromine tạo thành carboxylic acid.
Ví dụ: CH3CHO + Br2+ H2O → CH3COOH + 2HBr
b) Oxi hoá aldehyde bởi thuốc thử Tollens
Thuốc thử Tollens là phức chất của ion Ag+ với ammonia, có công thức [Ag(NH3)2]OH. Ion Ag+ trong thuốc thử Tollens đóng vai trò là chất oxi hóa:
RCHO +2[Ag(NH3)2]OH 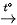 RCOONH4 +2Ag + 3NH3 + H20
RCOONH4 +2Ag + 3NH3 + H20
Ví dụ: CH3CHO + 2[Ag(NH3)2]OH 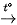
Phản ứng tạo thành lớp bạc sáng bóng bám vào bình phản ứng, vì vậy phản ứng này còn được gọi là phản ứng tráng bạc.
Ketone không bị oxi hoá bởi thuốc thử Tollens, vì vậy có thể dùng thuốc thử Tollens đề phân biệt aldehyde với ketone và các hợp chất khác.
| Hoạt động thí nghiệm Thí nghiệm phản ứng của aldehyde với thuốc thử Tollens Chuẩn bị: dung dịch CH3CHO 5%, dung dịch AgNO3 1%, dung dịch NH3 5%, cốc nước nóng, ống nghiệm. Tiến hành: - Cho khoảng 1 mL dung dịch AgNO3 1% vào ống nghiệm, thêm vài giọt dung dịch NaOH 10%. - Thêm từ từ dung dịch NH3 5% vào ống nghiệm và lắc đều đến khi kết tủa tan hoàn toàn. - Nhỏ vài giọt dung dịch CH3CHO 5% vào ống nghiệm, lắc đều. |
(Trang 141)
| - Đặt ống nghiệm vào cốc chứa nước nóng (khoảng 70 – 80 °C), đề yên khoảng 5 phút. Giải thích hiện tượng quan sát được và viết phương trình hoá học của phản ứng xảy ra. |
c) Oxi hoá aldehyde bằng copper(II) hydroxide
Aldehyde có thể bị oxi hoá bởi copper(II) hydroxide Cu(OH)2 trong môi trường kiềm khi đun nóng tạo thành kết tủa copper(I) oxide (Cu2O) màu đỏ gạch:
RCHO + 2Cu(OH)2 + NaOH 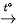 RCOONa + Cu2O + 3H2O
RCOONa + Cu2O + 3H2O
| Hoạt động nghiên cứu Nghiên cứu phản ứng oxi hoá aldehyde bằng copper(II) hydroxide Thí nghiệm oxi hoá CH3CHO bằng Cu(OH)2 được tiến hành như sau: - Cho khoảng 0,5 mL dung dịch CuSO, 5% và khoảng 1 mL dung dịch NaOH 10% vào ống nghiệm, lắc đều hỗn hợp. - Thêm khoảng 1 mL CH3CHO 5% vào ống nghiệm, lắc đều ống nghiệm. - Đun nóng nhẹ ống nghiệm trên ngọn lửa đèn cồn. Hỗn hợp phản ứng chuyển dần từ màu xanh lam sang màu đỏ gạch. Trả lời câu hỏi và thực hiện yêu cầu sau: 1. Khi cho dung dịch CuSO4 vào dung dịch NaOH, hỗn hợp tạo kết tủa màu xanh lam, kết tủa đó là chất gì? 2. Viết phương trình hoá học của các phản ứng xảy ra trong thí nghiệm trên.
Hình 23.6. Phản ứng của CH3CHO với CuSO4 trong dung dịch NaOH |
| CÂU HỎI VÀ BÀI TẬP 4. Viết phương trình hoá học của phản ứng giữa HCHO với các tác nhân sau: a) Thuốc thử Tollens; b) Cu(OH)2/NaOH. |
3. Phản ứng cộng
Hợp chất carbonyl có thể tham gia phản ứng cộng với HCN vào liên kết đôi C=O.
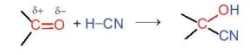
(Trang 142)
Ví dụ:
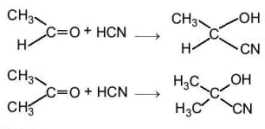
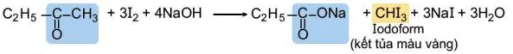
4. Phản ứng tạo iodoform
Các hợp chất aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl có thể phản ứng với 12 trong môi trường kiềm.
Ví dụ:
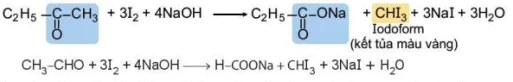
Iodoform (kết tủa màu vàng)
Phản ứng tạo sản phẩm kết tủa iodoform nên phản ứng này được gọi là phản ứng iodoform và được dùng để nhận biết các aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl.
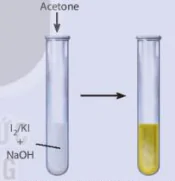
| Hoạt động nghiên cứu Nghiên cứu phản ứng tạo iodoform từ acetone Phản ứng tạo iodoform từ acetone được tiến hành như sau: - Cho khoảng 2 mL dung dịch 12 bão hoà trong Ki vào ống nghiệm. - Thêm khoảng 2 mL dung dịch NaOH 2 M. - Thêm tiếp khoảng 0,5 mL acetone vào hỗn hợp trên và lắc đều ống nghiệm, quan sát thấy xuất hiện kết tủa màu vàng. Viết phương trình hoá học của phản ứng xảy ra.
Hình 23.7. Phản ứng iodoform |
| CÂU HỎI VÀ BÀI TẬP 5. Hoàn thành các phản ứng sau: a) HCHO + HCN → b) CH3COCH(CH3)2 + I2 + NaOH→ 6. Trong các hợp chất sau, hợp chất nào tham gia phản ứng iodoform? a) metanol; b) etanol; c) butanon; d) pentan-3-one. |
(Trang 142)
Ví dụ:
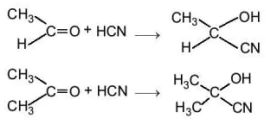
CH3
C=O + HCN
H
CH3
CH3
C=O + HCN
CH3
H
C
OH
CN
H3C
H3C
C
OH
CN
4. Phản ứng tạo iodoform
Các hợp chất aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl có thể phản ứng với 12 trong môi trường kiềm.
Ví dụ:
CH3-CHO + 3I2 + 4NaOH → H-COONa + CHI3 + 3NaI + H2O
C2H5
C
O
CH3
3I2
4NaOH
C2H5
C
ONa
O
CHI3
3NaI
3H2O
Iodoform
(kết tủa màu vàng)
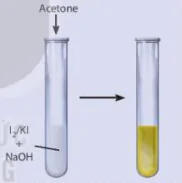
| Hoạt động nghiên cứu Nghiên cứu phản ứng tạo iodoform từ acetone Phản ứng tạo iodoform từ acetone được tiến hành như sau: - Cho khoảng 2 mL dung dịch 12 bão hoà trong Ki vào ống nghiệm. - Thêm khoảng 2 mL dung dịch NaOH 2 M. - Thêm tiếp khoảng 0,5 mL acetone vào hỗn hợp trên và lắc đều ống nghiệm, quan sát thấy xuất hiện kết tủa màu vàng. Viết phương trình hoá học của phản ứng xảy ra.
Hình 23.7. Phản ứng iodoform Acetone I2KI NaOH |
| CÂU HỎI VÀ BÀI TẬP 5. Hoàn thành các phản ứng sau: a) HCHO + HCN → b) CH3COCH(CH3)2 + I2 + NaOH→ 6. Trong các hợp chất sau, hợp chất nào tham gia phản ứng iodoform? a) methanal; b) ethanal; c) butanone; d) pentan-3-one. |
(Trang 143)
V. ỨNG DỤNG
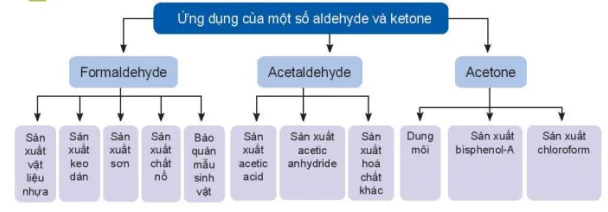
Ứng dụng của một số aldehyde và ketone
Formaldehyde
Acetaldehyde
Aceton
Sản xuất vật liệu nhựa
Sản xuất keo dán
Sản xuất son
Sản xuất chất no
Bảo quản mẫu sinh vật
Sản xuất acetic acid
Sản xuất acetic anhydride
Sản xuất hoá chất khác
Dung môi
Sản xuất bisphenol-A
Sản xuất chloroform
| Hoạt động nghiên cứu Hãy tìm hiểu và trình bày ứng dụng của một số aldehyde.
a) Keo phenolformaldehyde dùng trong công nghiệp gỗ dán
b) Các vật dụng được sản xuất từ nhựa melamine
c) Các mẫu sinh vật được bảo quản trong formol Hình 23.8. Một số ứng dụng của formaldehyde |
| Một lượng nhỏ acetone được tạo ra trong cơ thể con người qua quá trình chuyển hoá chất béo không hoàn toàn. Ở người khoẻ mạnh, acetone được hình thành ở gan và được chuyển hoá gần như hoàn toàn, chỉ có một lượng rất nhỏ xuất hiện trong nước tiểu. Sự hiện diện của acetone bắt thường trong nước tiểu là một dấu hiệu của bệnh tiểu đường và được phát hiện qua việc xét nghiệm nước tiều (chỉ số KET). |
VI. ĐIỀU CHẾ
Một số hợp chất carbonyl được tổng hợp trong công nghiệp bằng phương pháp oxi hoá các hydrocarbon, oxi hoá ethylene thành acetaldehyde, oxi hoá cumene thành acetone (quy trinh cumene, xem Bài 21. Phenol).
Ví dụ:
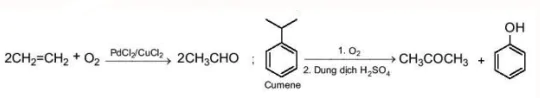
2CH2=CH2 + O2
PdCl2/CuCl2
2CH3CHO
Cumene
1. O2
2. Dung dịch H2SO4
CH3COCH3
OH
(Trang 144)
| EM ĐÃ HỌC
Ketone là hợp chất hữu cơ có nhóm
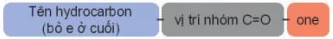
Aldehyde đơn chức: Tên hydrocarbon (bỏ e ở cuối) al Ketone đơn chức: Tên hydrocarbon (bỏ e ở cuối) vị trí nhóm C=O one
~120° C=O
Phản ứng khử: Aldehyde + 2[H] → Alcohol bậc I Ketone + 2[H] → Secondary Alcohol Phản ứng oxi hoá aldehyde: Aldehyde 101 Phản ứng cộng: Phản ứng tạo iodoform:
Idoform (kết tủa màu vàng)
|
| EM CÓ THỂ
|





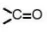

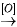 Carboxylic acid
Carboxylic acid








































































Bình Luận
Để Lại Bình Luận Của Bạn