Nội Dung Chính
[trang 111]
MỤC TIÊU
• Nêu được khái niệm về alkene.
• Viết được công thức cấu tạo và nêu được tính chất vật lí của ethylene.
• Trình bày được tính chất hóa học của ethylene (phần ứng cháy, phản ứng làm mặt màu nước bromine, phản ứng trùng hợp). Viết được các phương trình hóa học xảy ra..
• Tiến hành được thí nghiệm (hoặc quan sát thí nghiệm) của ethylene: phản ứng đốt cháy, phản ứng làm mất màu nước bromine, quan sát và giải thích được tính chất hóa học cơ bản của alkene.
• Trình bày được một số ứng dụng của ethylene: tổng hợp ethylic alcohol, tổng hợp nhựa polyethylene (PE).
Khí ethylene có tác dung thúc đẩy quá trình chín của trái cây. Ethylene thuộc loại hợp chất hữu cơ nào? Ethylene có cấu tạo, tính chất như thế nào và có vai trò gì trong công nghiệp hóa chất?
1 - Khái niệm alkene
Cho công thức cấu tạo của một số alkene như sau:
CH2═CH2 CH3__CH═CH2 CH3__CH═CH__CH3
Thực hiện các yêu cầu sau:
1. Nhận xét về đặc điểm chung của các công thức cấu tạo đã cho.
2. Viết công thức phân tử của các alkene trên, từ đó rút ra công thức chung của các alkene đó.
Alkene là nhüng hydrocarbon mạch hở, trong phân tử có một liên kết đôi 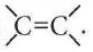
Công thức chung của các alkene có dang C,Hạn (với n ≥ 2, n là các số nguyên, dương).
II - Ethylene
1. Tính chất vật lí
Ethylene là chất khí ở điều kiện thường (hóá lỏng ở -104 °C và hóá răn ở -169 °C(1)), không màu, hầu như không tan trong nước, tan ít trong các dung môi hữu cơ như ethylic alcohol.
2. Cấu tạo phân tử
Công thức phân tử của ethylene là C2H4. Công thức cấu tạo của ethylene là 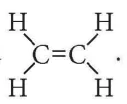
Phân tử ethylene có liên kết đôi 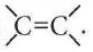 , trong đó có một liên kết kém bền, dễ bị phá vỡ trong các phản ứng hoá học.
, trong đó có một liên kết kém bền, dễ bị phá vỡ trong các phản ứng hoá học.
Nguồn: Haynes, W. M., Lide, D. R. & Bruno, T. J. 2017. CRC Handbook of Chemistry and Physics, 97th Edition, CRC Press LLC.
[trang 112]
3. Tính chất hóa học
Thí nghiệm: Điều chế và thử tính chất của ethylene
Chuẩn bị: bình cầu có nhánh 250ml đựng dung dịch cồn 96° và dung dịch H2S04, đặc đã được trộn đều, đã bọt, ống nghiệm chứa khoảng 2ml nước bromine, bình thuỷ tinh chứa dung dịch NaOH, ống dẫn thủy tinh đầu vuốt nhọn, ống dẫn thủy tinh hình chữ L.
Dụng cụ thí nghiệm được lắp sẵn như Hình 24.1.
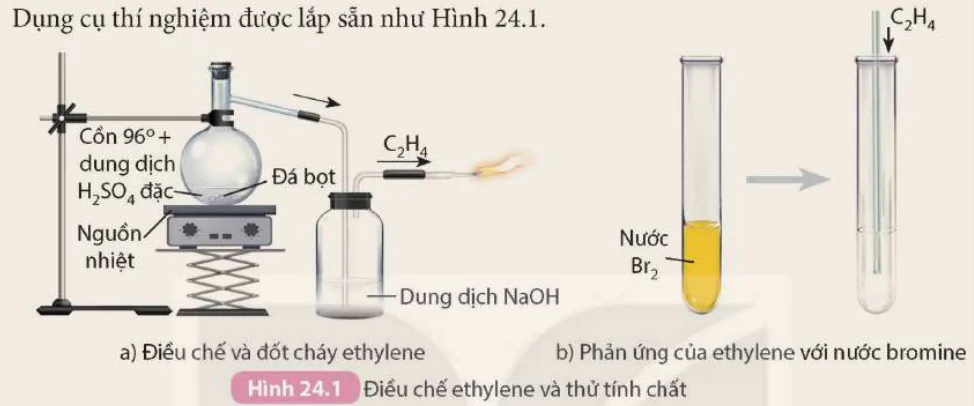
Hình 24.1 Điều chế ethylene và thử tính chất
Tiến hành:
⁃ Đun nóng bình cầu đến khi khí ethylene sinh ra và đi vào ống dẫn thủy tinh có đầu vuốt nhọn. Dùng que đóm đang cháy để đốt ethylene ở đầu vuốt nhọn của ống dẫn.
⁃ Thay ống dẫn thủy tinh đầu vuốt nhọn bằng ống dẫn thuỷ tinh hình chữ L. và dẫn khí ethylene vào ống nghiệm đựng nước bromine.
Thực hiện các yêu cầu sau:
Quan sát hiện tượng xảy ra ở đầu ống dẫn thủy tinh vuốt nhọn và tại ống nghiệm đựng nước bromine. Rút ra nhận xét về tính chất hóa học của ethylene.
a) Phản ứng cháy
Tương tự alkane, phản ứng đốt cháy các alkene tạo ra sản phẩm chủ yếu là khí carbon dioxide và hơi nước. Phản ứng toả ra nhiều nhiệt.
C2H4 +3O2 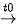 2CO2 + 2H2O
2CO2 + 2H2O
b) Phản ứng cộng
Trong phản ứng của ethylene với nước bromine, phân tử bromine đã cộng hợp vào nối đôi 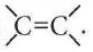
phẩm 1,2-dibromoethane theo phản ứng sau:
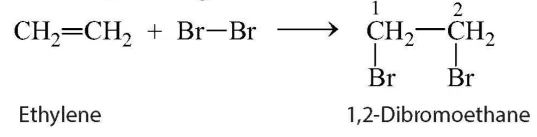
Viết gọn lại là: C2H4 +Br2 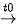 C2H4Br2
C2H4Br2
Phản ứng trên gọi là phản ứng cộng.
[trang 113]
c) Phản ứng trùng hợp
Ở điều kiện thích hợp, các phân tử ethylene cộng hợp liên tiếp với nhau, liên kết kém bền trong liên kết đôi của phân tử ethylene bị phá vỡ, tạo thành chất có khối lượng phân tử lớn, theo phương trình hóa học sau:
...CH2═CH2+CH2═CH2+CH2═CH2... 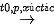 ... ─CH2─CH2─CH2─CH2─CH2─CH2─...
... ─CH2─CH2─CH2─CH2─CH2─CH2─...
Phản ứng trên gọi là phản ứng trùng hợp.
Phản ứng trùng hợp ethylene có thể viết như sau:
nCH2═CH2 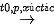 ─(CH2─CH2)─n
─(CH2─CH2)─n
Ethylene Polyethylene
Polyethylene (nhựa PE) là chất rắn, không tan trong nước, không độc, được dùng để sản xuất túi đựng, màng bọc, chai, bình chúa... Tuy nhiên, nhựa PE rất khó phân huỷ sinh học, có thể tồn tại bền trong môi trường hàng trăm năm, vì vậy cần giảm thiểu việc thải các sản phẩm làm từ nhựa PE ra ngoài môi trường.
❓ Propylene là một alkene, có công thức cấu tạo CH,-CH-CH,. Propylene có tính chất hóa học tương tự ethylene không? Tại sao? Viết các phương trình hóa học minh hoạ.
4. Ứng dụng
Ethylene là nguyên liệu quan trọng cho ngành công nghiệp sản xuất hóa chất và tổng hợp polymer (Hình 24.2).
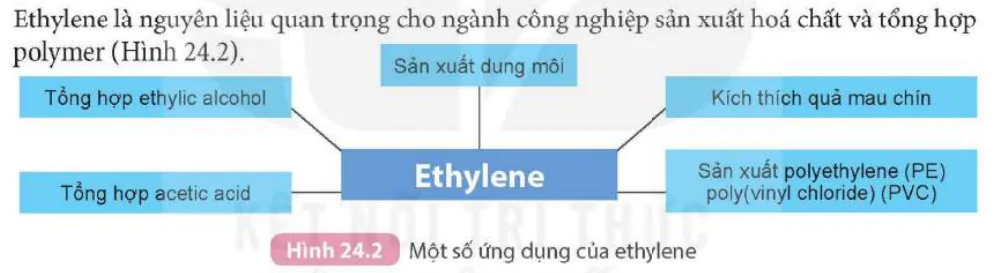
Hình 24.2 Một số ứng dụng của ethylene
Em hãy tìm các hình ảnh minh hoa và viết bài trình bày về các ứng dụng của ethylene.
EM ĐÃ HỌC
• Alkene là những hydrocarbon mạch hở, phân tử có một liên kết đối, công thức chung có dạng CnH2n (n ≥ 2, n là số nguyên, dương).
• Ethylene là chất khí, không màu, không mùi, ít tan trong nước.
• Ethylene và các alkene khác có các tính chất hóa học sau; tham gia phản ứng cộng, phản ứng trùng hợp, phản ting cháy,....
• Ethylene là một nguyên liệu quan trọng trong công nghiệp hóa chất và tổng hợp polymer.
EM CÓ THỂ
Nhận biết và lựa chọn được các sản phẩm làm từ nguyên liệu polyethylene và sử dụng chúng đúng cách để bảo vệ môi trường.
















































Bình Luận
Để Lại Bình Luận Của Bạn