(Trang 35)
MỤC TIÊU
- Nếu được khái niệm acid (tạo ra ion H+).
- Tiến hành được thí nghiệm của hydrochloric acid (làm đổi màu chất chỉ thị; phản ứng với kim loại), nêu và giải thích được hiện tượng xảy ra trong thí nghiệm (viết phương trình hoá học) và rút ra nhận xét về tính chất của acid.
- Trình bày được một số ứng dụng của một số acid thông dụng (HCI,
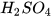 ,
,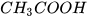 ).
).
Tại sao giấm ăn, nước quả chanh,... đều có vị chua và được dùng để loại bỏ cặn trong dụng cụ đun nước?
I- Khái niệm acid
Tìm hiểu khái niệm acid
Bảng 8.1. Tên một số acid thông dụng, công thức hoá học và dạng tồn tại của acid trong dung dịch.
| Tên acid | Công thức hóa học | Dạng tồn tại của acid trong dung dịch | |
| Cation (ion dương) | Anion (ion âm) Gốc acid | ||
| Hydrochloric acid | HCl | H+ | Cl- |
| Nitric acid | 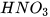 | H+ | 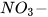 |
| Sulfuric acid | 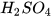 | H+ | 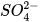 |
Quan sát Bảng 8.1 và thực hiện các yêu cầu:
1. Công thức hoá học của các acid có đặc điểm gì giống nhau?
2. Dạng tồn tại của acid trong dung dịch có đặc điểm gì chung?
3. Đề xuất khái niệm về acid.
(Trang 36)
Acid ban đầu được biết đến là những chất có vị chua như acetic acid có trong giấm ăn, citric acid có trong quả chanh, maleic acid có trong quả táo. Từ acid xuất phát từ tiếng Latin là acidus – nghĩa là vị chua. Khái niệm về acid được phát biểu như sau: Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion H+.
Hãy cho biết gốc acid trong các acid sau: 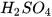 , HCl,
, HCl, 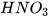
II – Tính chất hoá học
Acid thường tan được trong nước, dung dịch acid làm đổi màu giấy quỳ từ tím sang đỏ.
Khi dung dịch acid phản ứng với một số kim loại như magnesium, sắt, kẽm,... nguyên tử hydrogen của acid được thay thế bằng nguyên tử kim loại để tạo thành muối và giải phóng ra khí hydrogen(*):
Mg + 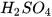 ----->
-----> 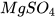 +
+ 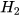
(Magnesium) (Sulfuric acid) (Magnesium sulfate) (Hydrogen)
Tính chất của dung dịch hydrochloric acid
Chuẩn bị: dung dịch HCl 1 M, giấy quỳ tím; hai ống nghiệm mỗi ống đựng một trong các kim loại Fe, Zn, ống hút nhỏ giọt.
Tiến hành:
- Nhỏ 1 – 2 giọt dung dịch HCl vào mẩu giấy quỳ tím.
- Cho khoảng 3 mL dung dịch HCl vào mỗi ống nghiệm đã chuẩn bị ở trên.
Mô tả hiện tượng xảy ra và viết phương trình hoá học.
Cho dung dịch HCl tác dụng với kim loại Mg. Viết phương trình hoá học của phản ứng xảy ra.
III – Một số acid thông dụng
1. Sulfuric acid
Sulfuric acid (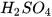 ) là chất lỏng không màu, không bay hơi, sánh như dầu ăn, nặng gần gấp hai lần nước. Sulfuric acid tan vô hạn trong nước và toả rất nhiều nhiệt.
) là chất lỏng không màu, không bay hơi, sánh như dầu ăn, nặng gần gấp hai lần nước. Sulfuric acid tan vô hạn trong nước và toả rất nhiều nhiệt.
Lưu ý: Tuyệt đối không tự ý pha loãng dung dịch sulfuric acid đặc.
Sulfuric acid là một trong các hoá chất được sử dụng nhiều trong các ngành công nghiệp (Hình 8.1) và là hoá chất được tiêu thụ nhiều nhất trên thế giới.
(*) Riêng 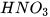 ,
, 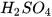 đặc tác dụng với kim loại sẽ được học sau.
đặc tác dụng với kim loại sẽ được học sau.
(Trang 37)
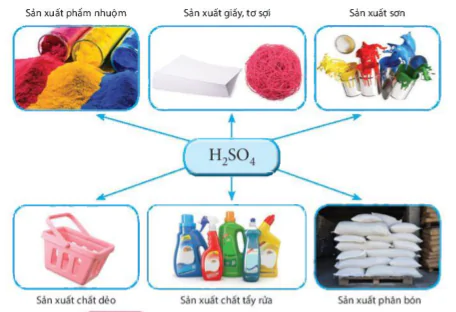
Sản xuất phẩm nhuộm
Sản xuất giấy, tơ sợi
Sản xuất sơn
Sản xuất chất dẻo
Sản xuất chất tẩy rửa
Sản xuất phân bón
Hình 8.1 Một số ứng dụng của sulfuric acid
Sử dụng Hình 8.1 để trình bày về các ứng dụng của sulfuric acid.
2. Hydrochloric acid
Dung dịch hydrochloric acid (HCl) là chất lỏng không màu.
Hydrochloric acid được sử dụng nhiều trong các ngành công nghiệp (Hình 8.2).

Tẩy gỉ thép Tổng hợp chất hữu cơ Xử lí pH nước bể bơi
Hình 8.2 Một số ứng dụng của hydrochloric acid
Sử dụng Hình 8.2 để trình bày về một số ứng dụng của hydrochloric acid.
Hydrochloric acid có trong dạ dày đóng vai trò quan trọng trong quá trình tiêu hoá như: thúc đẩy quá trình tiêu hoá thức ăn; kích thích ruột non và tuy sản xuất ra các enzyme tiêu hoá để phân giải chất béo, protein,...; tiêu diệt các vi khuẩn có hại từ bên ngoài đi vào dạ dày... Khi nồng độ acid trong dạ dày lớn hơn hoặc nhỏ hơn quá mức cần thiết đều gây ảnh hưởng đến chức năng tiêu hoá của dạ dày nói riêng và sức khoẻ nói chung.
(Trang 38)
3. Acetic acid
Acetic acid (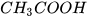 ) là chất lỏng không màu, có vị chua. Trong giấm ăn có chứa acetic acid với nồng độ 2 – 5%.
) là chất lỏng không màu, có vị chua. Trong giấm ăn có chứa acetic acid với nồng độ 2 – 5%.
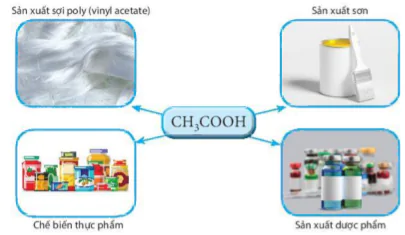
Sản xuất sợi poly (vinyl acetate)
Chế biến thực phẩm
Sản xuất sơn
Sản xuất dược phẩm
Hình 8.3 Một số ứng dụng của acetic acid
? Sử dụng Hình 8.3 để trình bày về các ứng dụng của acetic acid.
Tìm hiểu ứng dụng của một số acid quan trọng
1. Hãy tìm hiểu về nhu cầu sử dụng và ứng dụng của một trong các acid sau: HCI, 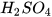 ,
, 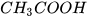 và trình bày trước lớp.
và trình bày trước lớp.
2. Việc sử dụng acid không đúng cách sẽ gây ô nhiễm môi trường đất, nước, không khí. Em hãy tìm hiểu về các tác hại này và trình bày trước lớp.
| EM ĐÃ HỌC | EM CÓ THỂ |
|
|








































Bình Luận
Để Lại Bình Luận Của Bạn